Les maladies hépato-biliaires chroniques, qu’elles soient d’origine métabolique, alcoolique, virale, auto-immune ou génétiques, sont caractérisées par l’association à divers degrés de phénomènes inflammatoires et de régénération, accompagnant le développement de lésions de stéatose, de fibrose, et l’apparition d’une cholestase. Globalement, la compréhension fine des mécanismes qui gouvernent ces processus aux échelons moléculaires, cellulaires et physiopathologiques reste indispensable pour établir les bases fondamentales de stratégies thérapeutiques visant à les contrôler. En effet, de façon critique, notre arsenal thérapeutique est dépourvu de traitements spécifiques efficaces anti-stéatosiques, anti-fibrosants, et modulateurs de l’homéostasie biliaire. C’est dans la perspective de découvrir de nouvelles cibles thérapeutiques pour ces maladies que s’inscrivent les projets de notre équipe.
Les quatre groupes de l'équipe 4 explorent le domaine biliaire – tant du côté des hépatocytes que des cholangiocytes – au travers de problématiques allant de la biologie cellulaire à la physiologie et la physiopathologie, jusqu'aux études cliniques et translationnelles.
La recherche translationnelle est un objectif crucial pour les quatre groupes, dans le contexte de la réparation hépatique, de la greffe, de la médecine régénérative, et des maladies pédiatriques.

Nos recherches visent à disséquer de nouvelles voies de signalisation régulant l'homéostasie biliaire pendant la les différents processus physiopathologiques du foie, qui pourraient être ciblées pour contrôler la composition et la taille du pool d’acides biliaires d’une part, ou les processus d'autophagie d’autre part.

Dans une démarche translationnelle, nos recherches sur modèles in vitro et in vivo visent à comprendre la physiopathologie de maladies cholestatiques rares et à identifier de nouvelles pistes thérapeutiques pharmacologiques.

Nos recherches visent à identifier les mécanismes cellulaires intervenant dans la différenciation et l'organisation tubulaire des cholangiocytes, avec pour objectif la construction de tubes biliaires dans une perspective de modélisation et d’études physiopathologiques.

Par des approches cellulaires, nous explorons l’effet de stress hépatocytaires sur les éléments du cytosquelette et la glycosylation de protéines circulantes. Le but est d’identifier des cibles thérapeutiques et des biomarqueurs précoces de souffrance cellulaire dans les maladies stéato-fibrosantes et lors de la conservation des greffons hépatiques.
Implications de la signalisation purinergique et des acides biliaires dans la physiopathologie des maladies hépato-biliaires.
Nos travaux ont pour objectif de mieux comprendre les mécanismes physiopathologiques régulant la réparation/régénération hépatique, avec la perspective d'ouvrir de nouveaux champs thérapeutiques dans la prise en charge des maladies du foie. Plus largement, notre groupe a acquis une forte expertise technique et conceptuelle dans les domaines de la régénération du foie, de l'homéostasie biliaire et des cholestases.
Au cours de la réparation du foie, les fonctions hépatiques doivent être maintenues pour préserver l’intégrité de l’organe et l’homéostasie de l’individu. Ceci est particulièrement crucial pour la sécrétion biliaire, dont la dérégulation entraîne une surcharge de l’organisme en acides biliaires (AB) avec ses conséquences toxiques sur le parenchyme hépatique. Les mécanismes de régulation de l’homéostasie biliaire au cours de la réparation du foie sont encore mal connus. La littérature ainsi que nos résultats indiquent que le système purinergique d’une part, ainsi que les AB d’autre part contribuent significativement à la régulation des processus de régénération cellulaire, de l’homéostasie biliaire, de la stéatogénèse et de la fibrogénèse au cours de la réparation du foie. Les deux axes scientifiques de nos projets sont :
L’objectif principal est de déterminer l’impact de la signalisation purinergique via le récepteur canal P2X4R sur la stéatogénèse et la fibrogénèse hépatiques, dans la perspective de découvrir de nouvelles cibles thérapeutiques pour les patients présentant une MAFLD (Metabolic Dysfunction Associated Fatty Liver Disease). Dans ce but nous utilisons des modèles expérimentaux in vitro et in vivo (souris), ainsi que des échantillons de patients.

L’objectif principal est de déterminer l’impact de la composition du pool d’AB sur la physiopathologie des maladies hépatobiliaires. Dans ce but nous utilisons des modèles expérimentaux in vitro et in vivo (souris), ainsi que l’analyse de prélèvements humains de patients dans différents contextes cliniques de régénération et réparation hépatique.

Physiopathologie et traitement des cholestases génétiques
La sécrétion biliaire est une fonction essentielle du foie, nécessaire à la digestion des graisses alimentaires et à l'élimination des xénobiotiques et des métabolites endogènes. Cette fonction dépend principalement de l'activité de transporteurs ABC (ATP-binding cassette), qui sont des protéines transmembranaires qui peuvent lier et hydrolyser l'ATP (adénosine triphosphate). Parmi ces transporteurs spécifiquement localisés au niveau de la membrane canaliculaire des hépatocytes, ABCB4 (aussi appelée MDR3, multidrug resistance protein type 3) permet la sécrétion de phosphatidylcholine (PC) dans la bile alors qu’ABCB11 (aussi appelée BSEP, bile salt export pump) transporte les sels biliaires et l'hétérodimère ABCG5/G8 transporte le cholestérol, l’ensemble de ces composants formant des micelles mixtes dans la bile (Figure 1, gauche). Ces transporteurs ABC sont des protéines transmembranaires dont les structures tridimensionnelles ont pu être récemment caractérisées, notamment par des approches de microscopie électronique cryogénique (Figure 1, droite).

À ce jour, plusieurs centaines de mutations des gènes encodant ces transporteurs ABC ont été identifiées chez des patients atteints de maladies hépatiques, dont une grande partie n’a pas été caractérisée aux échelles moléculaire et cellulaire. Les mutations d’ABCB4 et d’ABCB11 sont à l’origine de maladies hépatiques rares dont les formes les plus sévères sont les cholestases intrahépatiques familiales progressives de types 2 et 3 (PFIC2/3). Les PFICs se caractérisent par une cholestase (arrêt ou diminution de l’écoulement de la bile), un ictère (jaunisse) et un prurit (démangeaisons) modéré à sévère, et évoluent le plus souvent vers une insuffisance hépatique, nécessitant alors une transplantation hépatique.
Dans ce contexte, les objectifs de nos projets de recherche sont les suivants :

Ciliopathies et organogénèse biliaire
Stress Hépatocytaire et Physiopathologie Hépatobiliaire
Les hépatocytes sont susceptibles de subir de nombreux stress en situation physiologique et/ou pathologique, et doivent s'adapter en mettant en place des mécanismes moléculaires et cellulaires permettant leur survie ou leur élimination. Dans ce contexte, nos projets explorent 2 grands axes:
1- Rôles du cytosquelette et d’organites cellulaires comme senseurs de stress hépatique et médiateurs moléculaires des réponses cellulaires.
L’étude des réponses précoces de la cellule hépatique et de son microenvironnement à l’accumulation de lipides ou à la compression mécanique, rencontrées dans les maladies stéato-fibrosantes du foie (MASLD, MASH), mais aussi lors d’hépatectomies partielles ou de cholestases, a pour but d’identifier de nouvelles cibles thérapeutiques et de nouveaux biomarqueurs diagnostiques, pronostiques et prédictifs. Initialement menée sur des modèles cellulaires, cette étude s’étend également aux modèles murins et aux échantillons de patients.
Les effets de l’hypothermie sur le cytosquelette, condition mimant la conservation des greffons hépatiques avant transplantation, sont un autre axe d’étude de notre groupe. Les marqueurs de stress caractérisés à l’échelle de la cellule sont à présent explorés à l’échelle du tissu à partir de biopsies de foies pathologiques murins et humains. Ce projet translationnel (mené en collaboration avec le Pr Allard -chirurgien PU-PH de l’unité- et des membres du groupe de Thierry Tordjmann) permettra d’identifier de nouveaux biomarqueurs prédictifs et d’améliorer à terme la prise en charge des patients.

Antérieurement, nous avons élucidé des mécanismes d’adaptation au stress impliquant le cytosquelette qui s’appliquent à nos travaux actuels :

A/ Nous avons révélé dans des hépatocytes un mécanisme initiateur de résistance acquise aux taxanes, par lequel les filaments de septines relocalisent depuis les fibres de stress d’actine vers les microtubules qui retrouvent alors leur dynamique. Ce mécanisme implique un remodelage du cytosquelette médié par Cdc42 et ses effecteurs BORG.

B/ Nous avons montré que les stress créant des dommages aux microtubules stimulent la phosphorylation de la protéine de dynamique microtubulaire CLIP-170 (+TIP) pour préserver l’intégrité du cytosquelette et l’adapter au stress. Nos travaux ont également permis de mettre en évidence qu’en réponse à de nombreux stress (physique, chimique ou biologique), les MTs sont hyperacétylés ce qui constitue un marqueur de stress à la fois précoce et réversible. De plus, cette hyperacétylation contrôle la fission des mitochondries et le processus d’autophagie (en particulier, la mitophagie).

C/ Nous avons également montré que la fragmentation des mitochondries et l’agrégation protéique sont des marqueurs précoces de stress qui peuvent induire de l’autophagie permettant à ces entités cytotoxiques d’être dégradées et recyclées par les lysosomes.
2- Rôle du Golgi comme site de production de biomarqueurs circulants en situation de stress hépatique

La glycosylation des protéines circulantes nécessite l’activité d’enzymes, de transporteurs et de canaux localisés dans l’appareil de Golgi des hépatocytes.
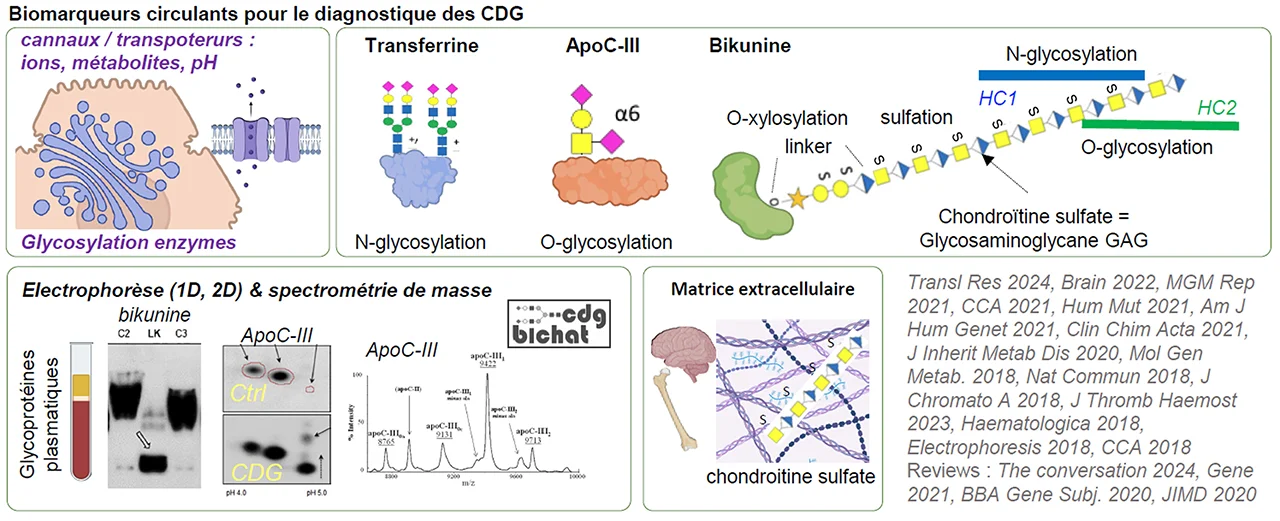
Nous avons montré que parmi ces glycoprotéines circulantes, la transferrine, l’apoliprotéine C-III et la bikunine permettent le diagnostic et le suivi thérapeutique des désordres congénitaux de la glycosylation (CDGs).
La bikunine est aussi un biomarqueur circulant pour les patients CDGs présentant une matrice extracellulaire anormale dans des tissus inaccessibles tels que le cerveau et les os.

Nous testons actuellement si ces biomarqueurs peuvent également servir dans les maladies stéato-fibrosantes acquises du foie. Pour l’aspect fibrosant, nous étudions le rôle du transfert des chaines lourdes (HC) de la bikunine sur l’acide hyaluronique des matrices extracellulaires. Enfin, nous allons étudier l’homéostasie golgienne des patients CDGs avec des mutations de la pompe V-ATPase, sachant que ces patients présentent une cholestase et une stéato-fibrose.
Nos travaux ont pour objectif de mieux comprendre les mécanismes physiopathologiques régulant la réparation/régénération hépatique, avec la perspective d'ouvrir de nouveaux champs thérapeutiques dans la prise en charge des maladies du foie. Plus largement, notre groupe a acquis une forte expertise technique et conceptuelle dans les domaines de la régénération du foie, de l'homéostasie biliaire et des cholestases.
Au cours de la réparation du foie, les fonctions hépatiques doivent être maintenues pour préserver l’intégrité de l’organe et l’homéostasie de l’individu. Ceci est particulièrement crucial pour la sécrétion biliaire, dont la dérégulation entraîne une surcharge de l’organisme en acides biliaires (AB) avec ses conséquences toxiques sur le parenchyme hépatique. Les mécanismes de régulation de l’homéostasie biliaire au cours de la réparation du foie sont encore mal connus. La littérature ainsi que nos résultats indiquent que le système purinergique d’une part, ainsi que les AB d’autre part contribuent significativement à la régulation des processus de régénération cellulaire, de l’homéostasie biliaire, de la stéatogénèse et de la fibrogénèse au cours de la réparation du foie. Les deux axes scientifiques de nos projets sont :
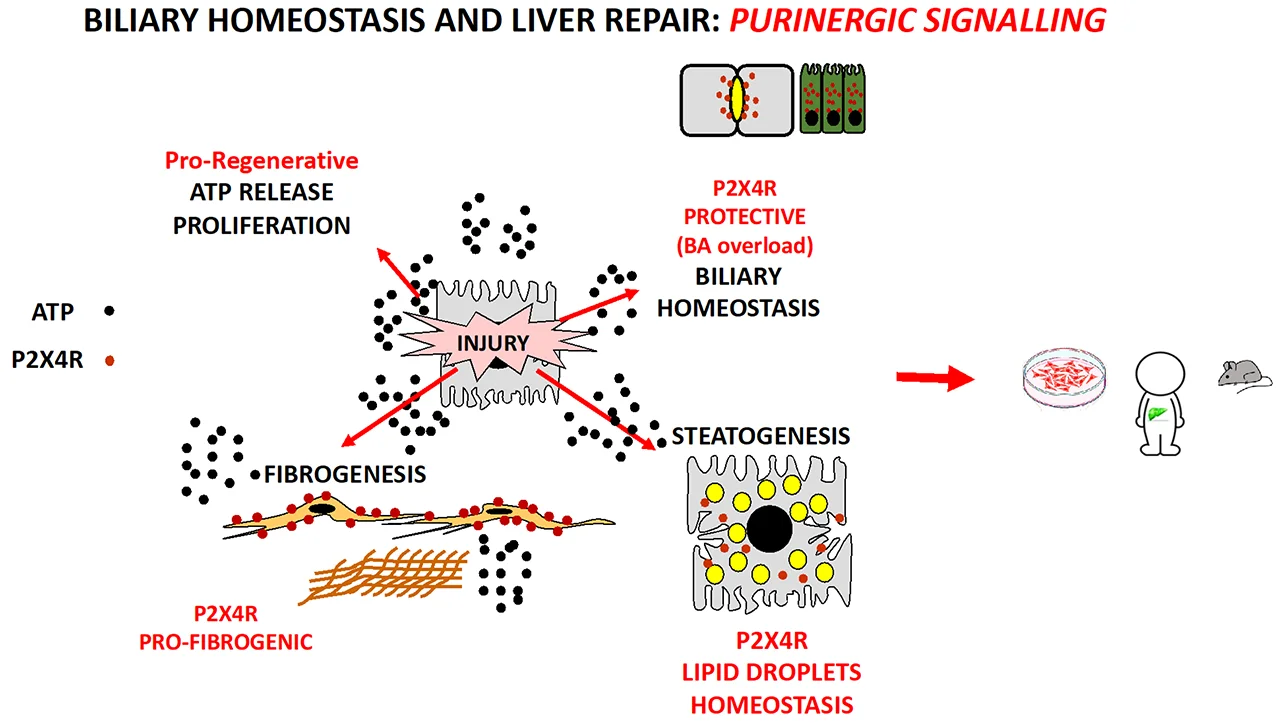
L’objectif principal est de déterminer l’impact de la signalisation purinergique via le récepteur canal P2X4R sur la stéatogénèse et la fibrogénèse hépatiques, dans la perspective de découvrir de nouvelles cibles thérapeutiques pour les patients présentant une MAFLD (Metabolic Dysfunction Associated Fatty Liver Disease). Dans ce but nous utilisons des modèles expérimentaux in vitro et in vivo (souris), ainsi que des échantillons de patients.
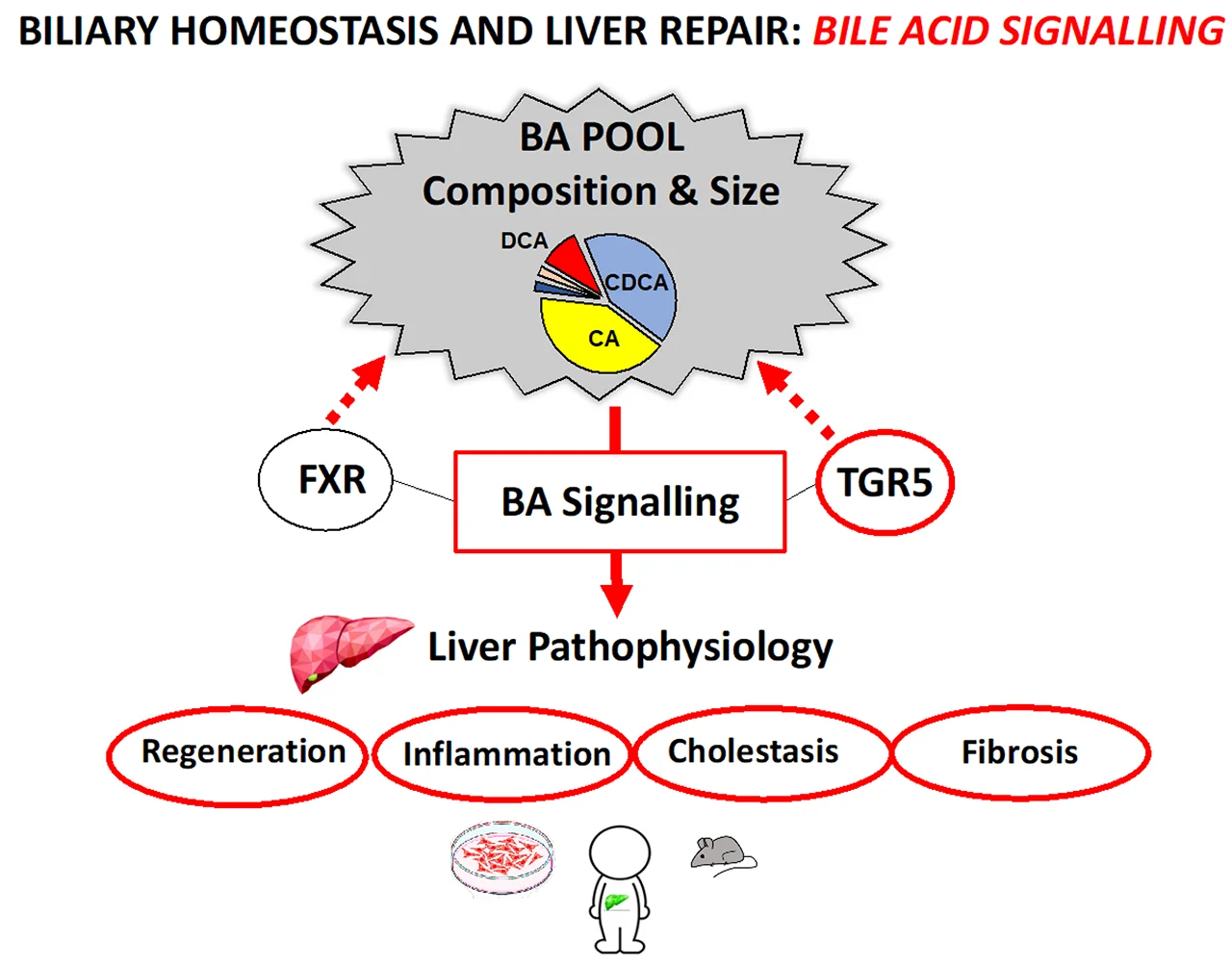
L’objectif principal est de déterminer l’impact de la composition du pool d’AB sur la physiopathologie des maladies hépatobiliaires. Dans ce but nous utilisons des modèles expérimentaux in vitro et in vivo (souris), ainsi que l’analyse de prélèvements humains de patients dans différents contextes cliniques de régénération et réparation hépatique.
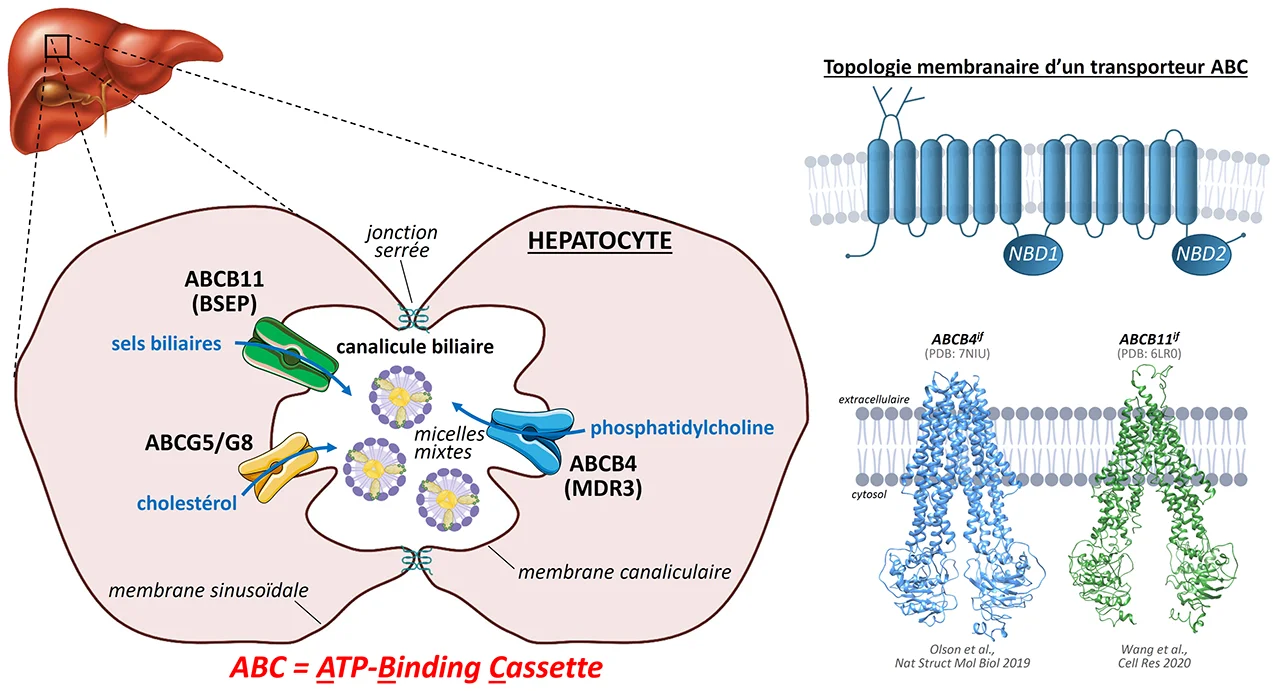
La sécrétion biliaire est une fonction essentielle du foie, nécessaire à la digestion des graisses alimentaires et à l'élimination des xénobiotiques et des métabolites endogènes. Cette fonction dépend principalement de l'activité de transporteurs ABC (ATP-binding cassette), qui sont des protéines transmembranaires qui peuvent lier et hydrolyser l'ATP (adénosine triphosphate). Parmi ces transporteurs spécifiquement localisés au niveau de la membrane canaliculaire des hépatocytes, ABCB4 (aussi appelée MDR3, multidrug resistance protein type 3) permet la sécrétion de phosphatidylcholine (PC) dans la bile alors qu’ABCB11 (aussi appelée BSEP, bile salt export pump) transporte les sels biliaires et l'hétérodimère ABCG5/G8 transporte le cholestérol, l’ensemble de ces composants formant des micelles mixtes dans la bile (Figure 1, gauche). Ces transporteurs ABC sont des protéines transmembranaires dont les structures tridimensionnelles ont pu être récemment caractérisées, notamment par des approches de microscopie électronique cryogénique (Figure 1, droite).
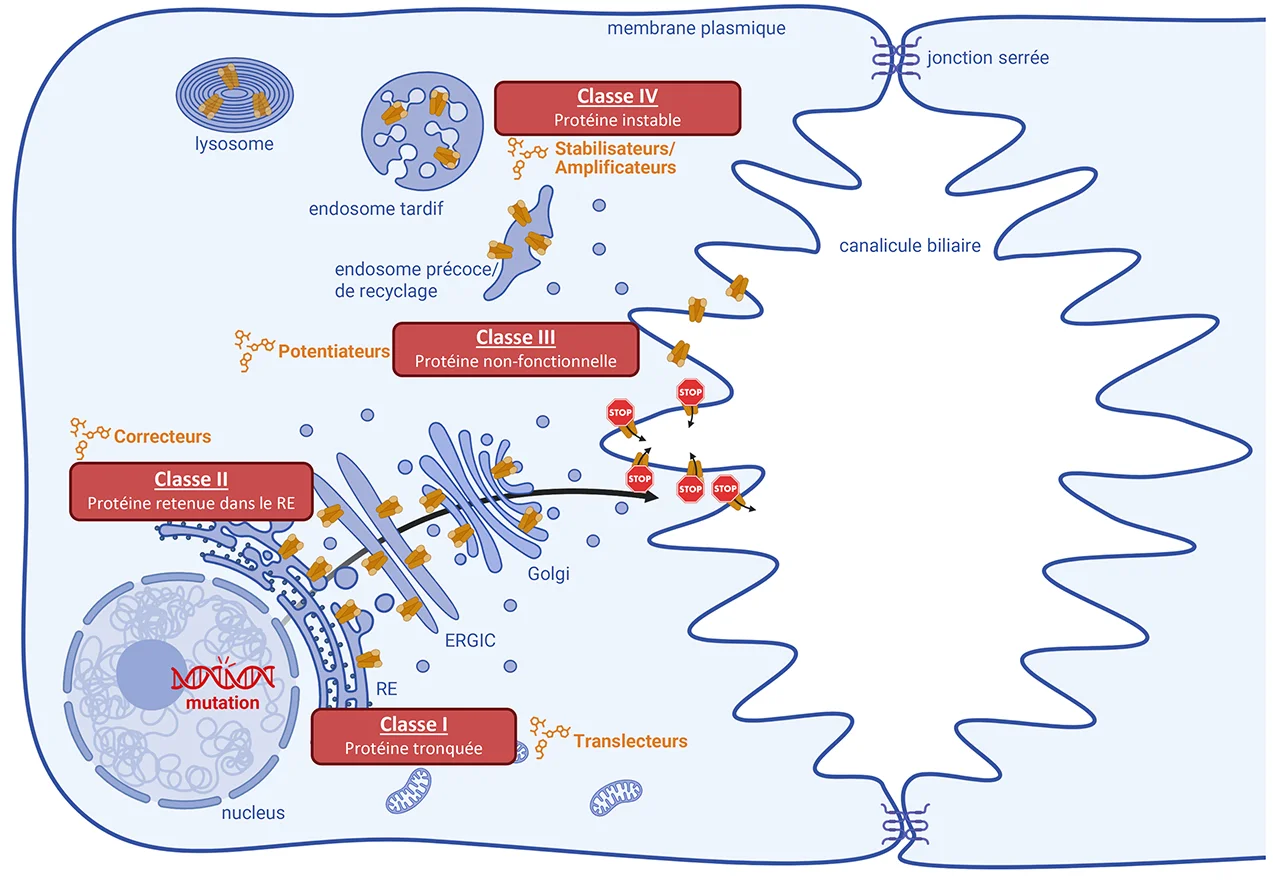
À ce jour, plusieurs centaines de mutations des gènes encodant ces transporteurs ABC ont été identifiées chez des patients atteints de maladies hépatiques, dont une grande partie n’a pas été caractérisée aux échelles moléculaire et cellulaire. Les mutations d’ABCB4 et d’ABCB11 sont à l’origine de maladies hépatiques rares dont les formes les plus sévères sont les cholestases intrahépatiques progressives de types 2 et 3 (PFIC2/3). Les PFICs se caractérisent par une cholestase (arrêt ou diminution de l’écoulement de la bile), un ictère (jaunisse) et un prurit (démangeaisons) modéré à sévère, et évoluent le plus souvent vers une insuffisance hépatique, nécessitant alors une transplantation hépatique.
Dans ce contexte, les objectifs de nos projets de recherche sont les suivants :
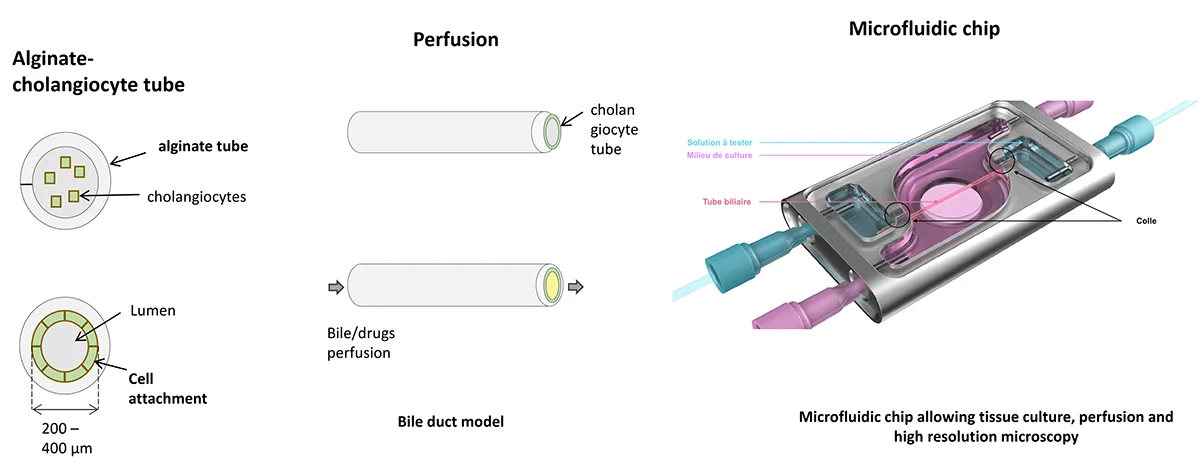
La construction au cours de l’embryogenèse et le maintien d’un système biliaire fonctionnel impliquent notamment le cil primaire, dont des dysfonctions sont associées à des ciliopathies biliaires. Bien que de nombreux travaux aient permis d’élucider le rôle du cil primaire des cholangiocytes dans la signalisation et la régulation de l’homéostasie biliaire, sa fonction dans l’organogénèse biliaire reste à élucider. Dans ce contexte, nous développons nos travaux selon deux axes : i) un programme de recherche destiné à décrypter le rôle des protéines du cil primaire dans la polarité épithéliale des cholangiocytes ; et ii) une activité de bioingénierie visant à la construction de tubes biliaires pour fournir des modèles de développement des voies biliaires in vitro et des outils pour la médecine régénérative.
Les hépatocytes sont susceptibles de subir de nombreux stress en situation physiologique et/ou pathologique, et doivent s'adapter en mettant en place des mécanismes moléculaires et cellulaires permettant leur survie ou leur élimination. Dans ce contexte, nos projets explorent 2 grands axes:
1- Rôles du cytosquelette et d’organites cellulaires comme senseurs de stress hépatique et médiateurs moléculaires des réponses cellulaires.
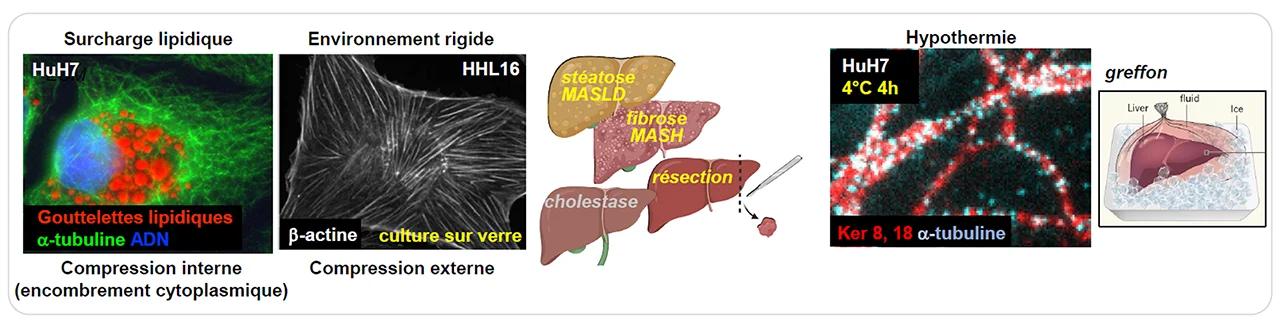
L’étude des réponses précoces de la cellule hépatique et de son microenvironnement à l’accumulation de lipides ou à la compression mécanique, rencontrées dans les maladies stéato-fibrosantes du foie (MASLD, MASH), mais aussi lors d’hépatectomies partielles ou de cholestases, a pour but d’identifier de nouvelles cibles thérapeutiques et de nouveaux biomarqueurs diagnostiques, pronostiques et prédictifs. Initialement menée sur des modèles cellulaires, cette étude s’étend également aux modèles murins et aux échantillons de patients.
Les effets de l’hypothermie sur le cytosquelette, condition mimant la conservation des greffons hépatiques avant transplantation, sont un autre axe d’étude de notre groupe. Les marqueurs de stress caractérisés à l’échelle de la cellule sont à présent explorés à l’échelle du tissu à partir de biopsies de foies pathologiques murins et humains. Ce projet translationnel (mené en collaboration avec le Pr Allard -chirurgien PU-PH de l’unité- et des membres du groupe de Thierry Tordjmann) permettra d’identifier de nouveaux biomarqueurs prédictifs et d’améliorer à terme la prise en charge des patients.
Antérieurement, nous avons élucidé des mécanismes d’adaptation au stress impliquant le cytosquelette qui s’appliquent à nos travaux actuels :
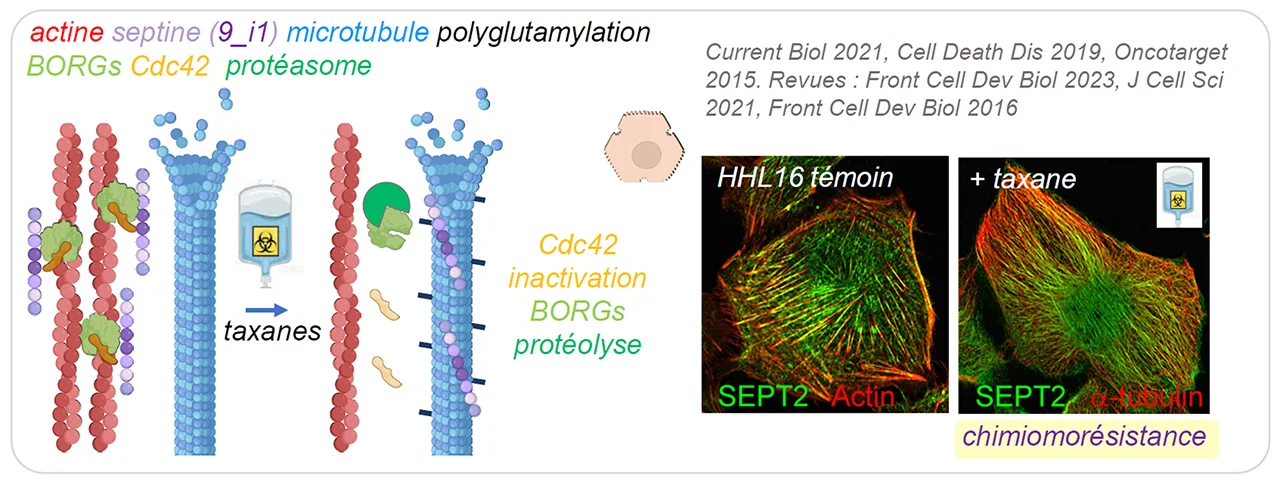
A/ Nous avons révélé dans des hépatocytes un mécanisme initiateur de résistance acquise aux taxanes, par lequel les filaments de septines relocalisent depuis les fibres de stress d’actine vers les microtubules qui retrouvent alors leur dynamique. Ce mécanisme implique un remodelage du cytosquelette médié par Cdc42 et ses effecteurs BORG.
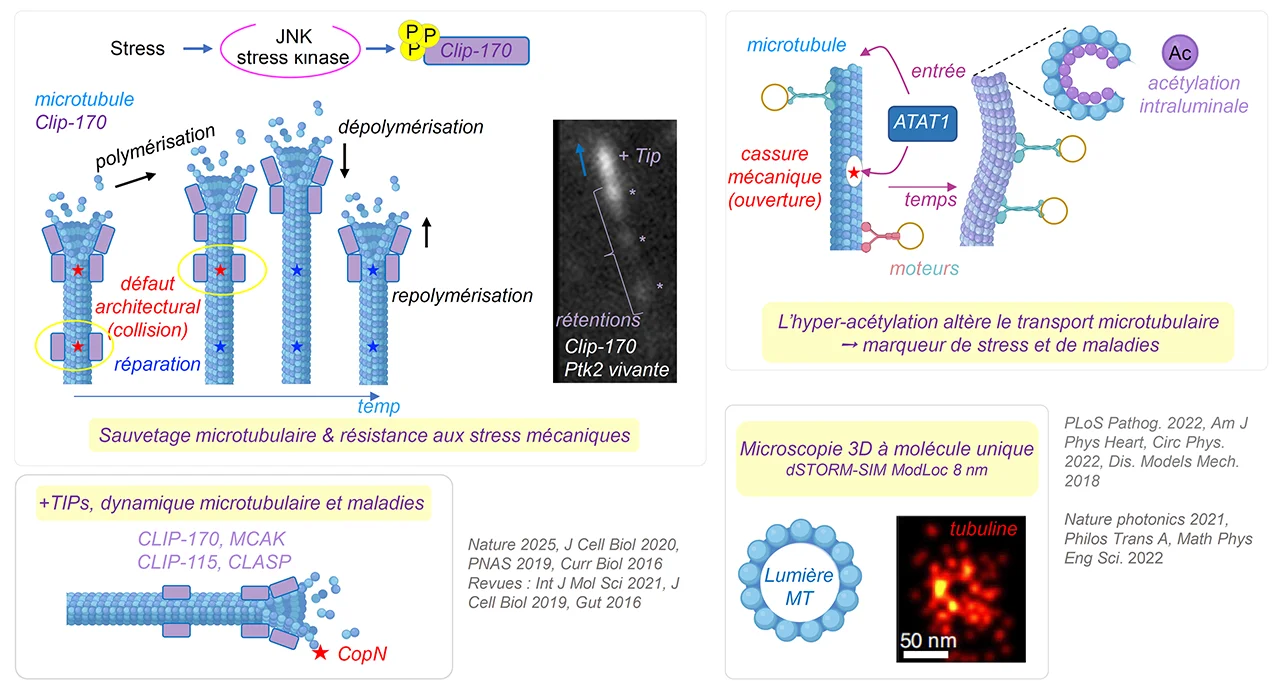
B/ Nous avons montré que les stress créant des dommages aux microtubules stimulent la phosphorylation de la protéine de dynamique microtubulaire CLIP-170 (+TIP) pour préserver l’intégrité du cytosquelette et l’adapter au stress. Nos travaux ont également permis de mettre en évidence qu’en réponse à de nombreux stress (physique, chimique ou biologique), les MTs sont hyperacétylés ce qui constitue un marqueur de stress à la fois précoce et réversible. De plus, cette hyperacétylation contrôle la fission des mitochondries et le processus d’autophagie (en particulier, la mitophagie).
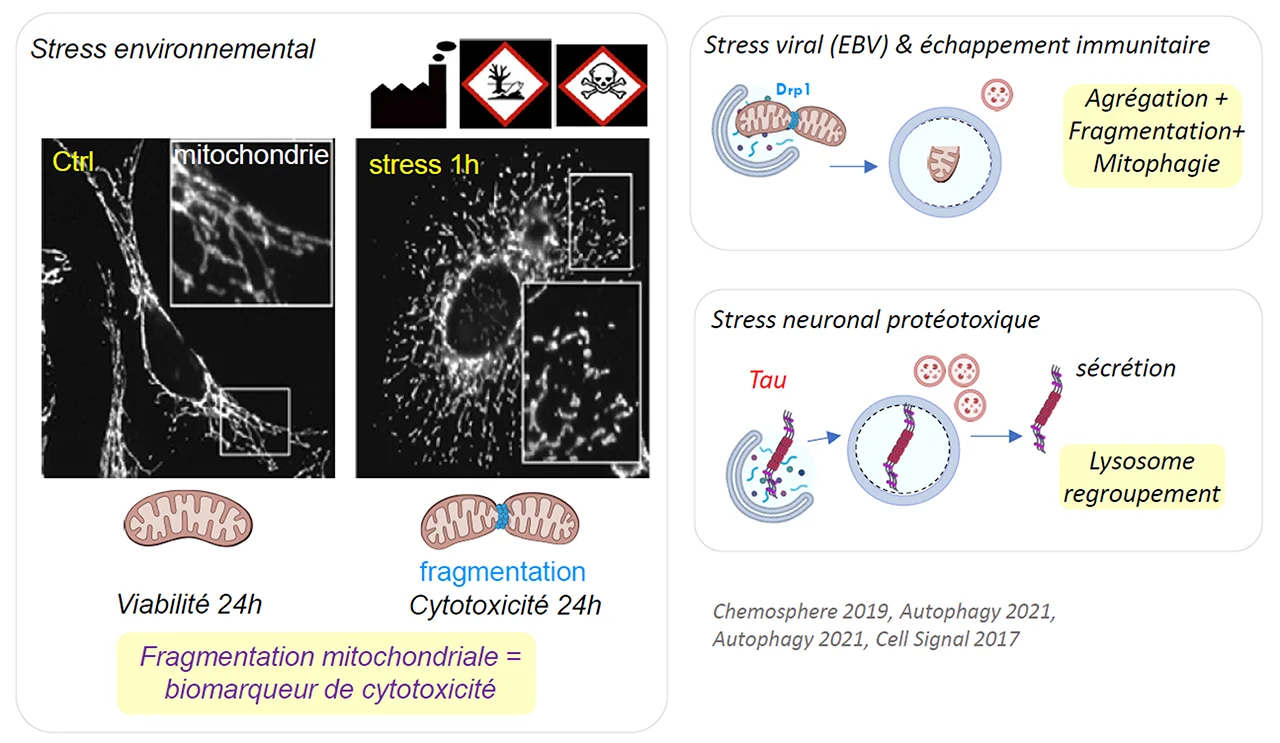
C/ Nous avons également montré que la fragmentation des mitochondries et l’agrégation protéique sont des marqueurs précoces de stress qui peuvent induire de l’autophagie permettant à ces entités cytotoxiques d’être dégradées et recyclées par les lysosomes.
2- Rôle du Golgi comme site de production de biomarqueurs circulants en situation de stress hépatique
La glycosylation des protéines circulantes nécessite l’activité d’enzymes, de transporteurs et de canaux localisés dans l’appareil de Golgi des hépatocytes.
Nous avons montré que parmi ces glycoprotéines circulantes, la transferrine, l’apoliprotéine C-III et la bikunine permettent le diagnostic et le suivi thérapeutique des désordres congénitaux de la glycosylation (CDGs).
La bikunine est aussi un biomarqueur circulant pour les patients CDGs présentant une matrice extracellulaire anormale dans des tissus inaccessibles tels que le cerveau et les os.
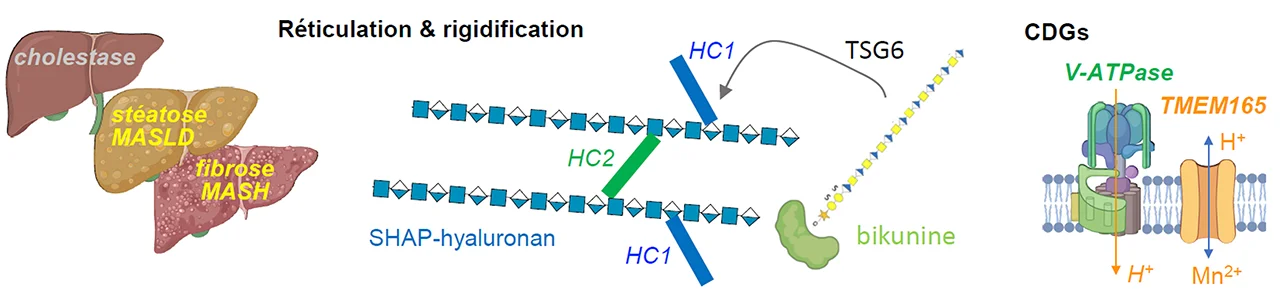
Nous testons actuellement si ces biomarqueurs peuvent également servir dans les maladies stéato-fibrosantes acquises du foie. Pour l’aspect fibrosant, nous étudions le rôle du transfert des chaines lourdes (HC) de la bikunine sur l’acide hyaluronique des matrices extracellulaires. Enfin, nous allons étudier l’homéostasie golgienne des patients CDGs avec des mutations de la pompe V-ATPase, sachant que ces patients présentent une cholestase et une stéato-fibrose.